|
�S�@�R���C�h�� �y�R���C�h�z �R���C�h���q �@�H�����Ȃǂ̗n�t�́C�n�����q�͗n�}���q�Ƃقړ����x�̑傫���������C�n���͗n�}�ɗn������ł���B���̂悤�ȗn�t��^�̗n�t�Ƃ����B����C���a�k�@10�|9�@�lm�`�k�@10�|7�@�lm���x�̔�r�I�傫�ȗ��q���k�@�R���C�h���q�@�l�Ƃ����C�R���C�h���q���t�̒��ɋψ�ɕ��U�������̂��R���C�h�n�t�Ƃ����B�R���C�h�n�t�ł̓R���C�h���q�U�i�n�����Ă���̂ł͂Ȃ��j�����Ă���t�̂U�}�C���U���Ă���R���C�h���q�U���Ƃ����B�܂��R���C�h�̒��ŗ������̂�����̂��k�@�]���@�l�C���������Ȃ����ő̏�̂��̂��k�@�Q���@�l�C������������������̂��k�@�L�Z���Q���@�l�Ƃ����B ��j�����F�]���@�����F�Q���@���쓤���F�L�Z���Q�� |
|
|
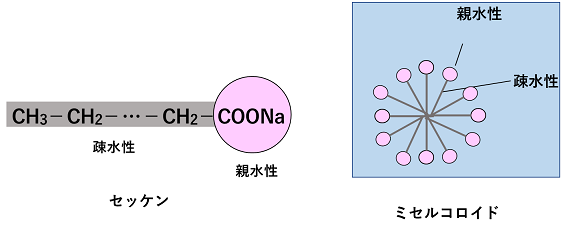
�R���C�h���q�̕��� �@�f���v����^���p�N���̂悤�ȍ����q�������͕��q1�ŃR���C�h���q�̑傫�������B���̂悤�ȃR���C�h���k�@���q�R���C�h�@�l�Ƃ����B �Z�b�P�����q�͐e����i���ɗn���₷�������Ɓj�Ƒa����i���ɗn���ɂ��������j����Ȃ�C�n�t���ł͑a���������ɁC�e������O���Ɍ�����悤�ɂ��āC50�`100���q�W�܂��ăR���C�h���q������B���̂悤�ȃR���C�h���k�@��R���C�h�@�l�܂��́k�@�~�Z���R���C�h�@�l�Ƃ����B�@ |
 |
|
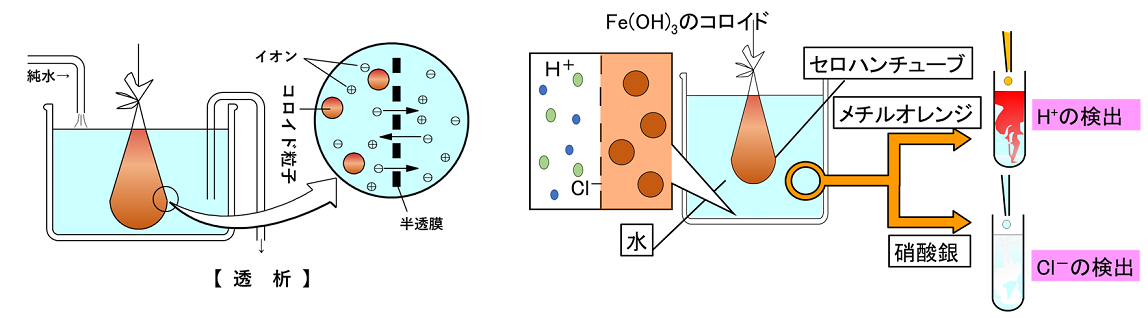
�����C�Y�f�C�S�y�Ȃǂ̕s�n�������́C�R���C�h���q�̑傫���ɂȂ��ĕ��U���Ă���B���̂悤�ȃR���C�h���k�@���U�R���C�h�@�l�Ƃ����B �y�R���C�h�n�t�̐����z ���� �������ɏ��ʂ̉����S(�V)FeCl3�̖O�a���n�t��������ƁC���̂悤�Ȕ������N����C�Ԋ��F�̐��_���S(�V)Fe(OH)3�̃R���C�h�n�t��������BFe(OH)3�͏W�܂��Ĉꕔ��OH��OH�̊Ԃ�H2O���Ƃ�Č������R���C�h���q�ƂȂ��B �@�k�@FeCl3�@�{�@3H2O�@���@Fe(OH)3�@�{�@3HCl�@�l ���̂悤�ɂ��Ă������R���C�h�n�t�ɂ́CFe(OH)3�̃R���C�h���q�̂ق��C�s�����Ƃ���H�{��Cl�|���܂܂��B���̍��������Z���n���̂悤�Ȕ������ɕ��ŏ����ɂ��Ă����ƁCH�{��Cl�|�͖���ʂ��Đ����֊g�U���Ă������CFe(OH)3�̃R���C�h���q�̓Z���n���̌������傫���̂Ő����֏o�Ă����Ȃ��B���̂悤�ɁC�������𗘗p���ăR���C�h�n�t���̕s����������������k�@�����@�l�Ƃ����B |
|
 |
|
|
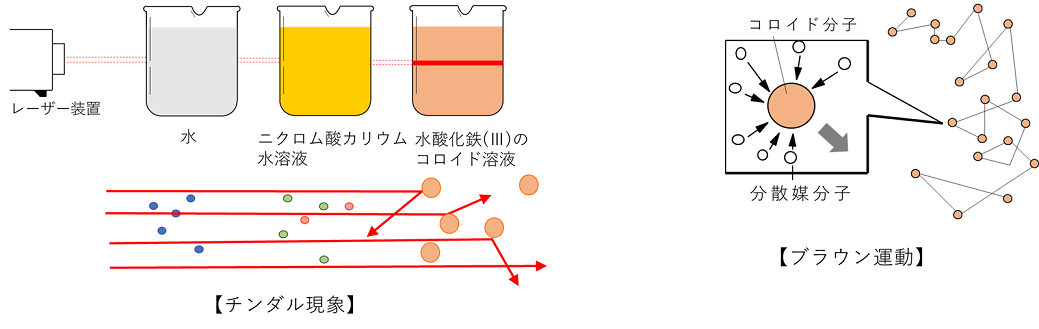
���⑫���@�Z���n���̊O���̐��Ɂk�@�Ɏ_���@�l���n�t��������ƁC�k�@�������@�l���������������邱�Ƃ���k�@Cl�|�@�l�̑��݂��C�k�@���`���I�����W�@�l��������ƐԐF�ɕω����邱�Ƃ���k�@H�{�@�l�̑��݂��m�F���邱�Ƃ��ł���B �`���_������ �@�R���C�h�n�t�ɉ����烌�[�U�[�����Ȃǂ̋������Ă�ƌ��̒ʘH�����邭�P���Č�����B���̌��ۂ��k�@�`���_�������@�l�Ƃ����B����̓R���C�h���q���傫���C���̕\�ʂŌ����悭�k�@�U���@�l����邽�߂ł���B����ɑ��ʏ�̗n�t�ł͗n�����q�������Ə��������߁C���͂قƂ�ǎU������Ȃ��B |
|
 |
|
|
�u���E���^�� �R���C�h�n�t�����O�������Ŋώ@����ƁC�R���C�h���q���̂��̎��̂͌����Ȃ����C�R���C�h���q�͏����Ȍ��̓_�Ƃ��Ă��̑��݂��ώ@�ł���B���̂Ƃ����̓_�͕s�K���ȃW�O�U�O�^�������Ă���̂�������B���̃R���C�h���q�̓������k�@�u���E���^���@�l�Ƃ����B����́k�@�M�^���@�l�����Ă���n�}���q���₦���R���C�h���q�ɏՓ˂��邽�߂ɋN����C���̂��߃R���C�h���q�͒��~���Ȃ��B |
|
|
�d�C�j���@ |
 |
|
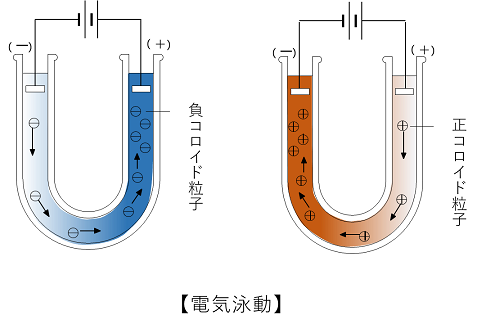
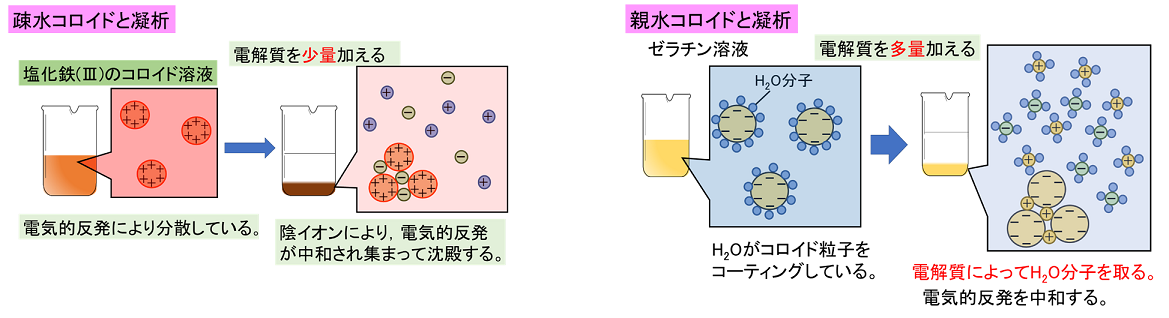
�a���R���C�h�ƋÐ� �@���Ƃ̐e�a�͂̎ア�i�\�ʂɐ����q�������t����͂��ア�j�R���C�h���k�@�a���R���C�h�@�l�Ƃ����B�a���R���C�h�́k�@�d�C�I�����@�l�ɂ���ėn�t���Œ��a���邱�ƂȂ�����ɕ��U��ۂ��Ă���B�@ �a���R���C�h�ɏ��ʂ̓d������������ƁC�ѓd���Ă����R���C�h���q�ɂ���Ɣ��Ε����̃C�I�����������������C�R���C�h���q�̑ѓd���d�C�I�ɒ��a������B���̂��߁C����܂ł̔����͂��Ȃ��Ȃ�C���q�ԗ͂��傫���Ȃ邽�߁C�R���C�h���q�݂͌��Ɍ������Ē��a����B���̂悤�����ʂ̓d�����Œ��a���錻�ۂ��k�@�Ð��@�l�Ƃ����B �@�R���C�h���q���Ð͂�����͂́C�������d�������琶����C�I���̉����ɂ��قȂ�B���Ȃ킿�C�R���C�h���q�Ɣ��Ε����̃C�I���ʼn����̑傫���C�I���قǁC�Ð͂�����\�͂��傫���Ȃ��B�Ⴆ�C���R���C�h�ł���Fe(OH)3�ɑ��Ắk�@Cl�|�@�l���@�@�@�k�@SO42�|�@�l���܂ޓd�����̕����L���ł���B |
|
 |
|
|
�e���R���C�h�Ɖ��� �@�f���v����[���`���Ȃǂ̃R���C�h�n�t�͏��ʂ̓d�����������Ă����a���Ȃ��B�����̃R���C�h���q�́C�k�@�e���R���C�h�@�l�Ƃ����C���̕\�ʂɐ����q�����������t���Ă���B���̂��߁C�e���R���C�h�𒾓a�����邽�߂ɂ́C���ʂ̓d�����������C�\�ʂ̐����q����菜���Ȃ���Ȃ�Ȃ��B���̂悤�ɁC�e���R���C�h�����ʂ̓d�����ɂ���Ē��a���錻�ۂ��k�@�����@�l�Ƃ����B�����̂ɂ���Ȃǂ����̗͂�ł��� �ی�R���C�h �@�a���R���C�h�ɐe���R���C�h��������ƁC�a���R���C�h�̗��q���e���R���C�h�̗��q�Ɏ��͂܂�C�Ð͂��ɂ����Ȃ�ꍇ������B���̂悤�ȕی��p���s���e���R���C�h���k�@�ی�R���C�h�@�l�Ƃ����B�Ⴆ�C�n�`�͑a���R���C�h�ŕs����ȒY�f�̃R���C�h�ɑ��āC�e���R���C�h�ł���j�J����ی�R���C�h�Ƃ��ĉ����Ă���B ����@���� (1) �` (5) �̋L�q�ɊY�����錻�ۂ⑀�얼���L���B (1)�@�R���C�h�ɋ������Ă�ƁC���̒ʘH���P���Č����錻�ہB (2)�@�����d�����������Ƃ��C�R���C�h���q���d�ɂɌ������ē������ہB (3)�@��������p���āC�R���C�h���q�Ƒ��̕��q��C�I�������鑀��B (4)�@�e���R���C�h�̗n�t�ɑ��ʂ̓d�����������Ē��a�����鑀��B (5)�@�R���C�h���q�����U�}���q�ɏՓ˂���ċN����s�K���ȉ^���B
����@���̕����́i�@�@�j�ɓK������C���̊e�₢�ɓ�����B �@�����S(�V)���n�t�������ɓ����ƁC���_���S(�V)�̃R���C�h�n�t���������B���̗n�t���Z���n���܂ɓ���C���������ɐZ���Ă����ƑO�������x�̍����n�t��������B���̑�����i
�A �j�Ƃ����C���̂Ƃ��̃Z���n���܂̊O�̐��n�t�́i �C �j���������B�����̃R���C�h�n�t�̈ꕔ���Ƃ�C�A���ʂ̓d�������n�t�������ĕ��u����ƒ��a���������B���̌��ۂ��i �E �j�Ƃ����B���̌��ۂ��N����₷�����Ƃ���C���_���S(�V)�̃R���C�h�́i �G �j�R���C�h�Ƃ�����B �@�܂��C���_���S(�V)�̃R���C�h�n�t�ɒ����d����������ƃR���C�h���q�͉A�ɑ��Ɉړ�����̂ŁC���̃R���C�h�́i �I �j�ɑѓd���Ă��邱�Ƃ��킩��B (1)�@�������@�̕ω������w�������Ŏ����B (2)�@�������A�ŁC���������Z�x�̓d�������n�t�̂����C�ł����ʂł��ނ��̂͂ǂꂩ�B1�I�сC�L���œ�����B �@�@�@�@�@KCl�@�@�A�@MgSO4�@�@�B�@AlCl3�@�@�C�@Na3PO4 (�A)�@���́@(�C)�@�_�@(�E)�@�Ð́@(�G)�@�a���@(�I)�@�� (1)�@FeCl3�{3H2O��Fe(OH)3�{3HCl�@ (2)�@Fe(OH)3�͉A�ɂɈړ�����̂ŁC���̃R���C�h�B �|�ʼn����̑傫�ȃC�I�����o����́@�@�@Cl�|�@�A�@SO42�|�@�B�@3Cl�|�@�C�@PO43�| �@�C ���n�t�̒����ƔZ�x�Ɋւ����聄 |
|
 |
|
|
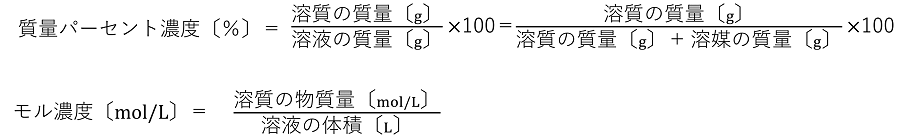
1�@���̊e�₢�ɓ�����BH��1.0�CC��12�CO=16�CNa��23�CS��32 (1)�@�A�f5.0g��45g�ɗn���������n�t�̎��ʃp�[�Z���g�Z�x�͉������B (2)�@10���̉����i�g���E�����n�t180g��20���̉����i�g���E�����n�t120g�������������n�t�̎��ʃp�[�Z���g�Z�x�͉������B (3)�@9.0g�̃O���R�[�XC6H12O6�𐅂ɗn������200mL�ɂ������n�t�͉�mol/L���B (4)�@0.25mol/L�̐��_���i�g���E��NaOH���n�t200mL���ɁCNaOH�͉�mol�܂܂�邩�B�܂��C�܂܂��NaOH�̎��ʂ͉�g���B (5)�@0.10mol/L�̗��_���n�t100mL��0.30mol/L�̗��_���n�t300mL�������������n�t�̃����Z�x�͉�mol/L���B (1)�@10���@(2)�@14���@(3)�@0.25mol/L�@(4)�@0.050mol/L�@2.0g�@(5)�@0.25mol/L 2�@���̊e�₢�ɓ�����BH2SO4��98�CHCl��36.5 (1)�@0.20mol/L���_���n�t(���x1.05g/cm3)�̎��ʃp�[�Z���g�Z�x�͉������B (2)�@�Z�x36.5���C���x1.2g/cm3�̔Z���_HCl�̃����Z�x�͂����炩�B (3)�@10���Z���_���n�t��p���āC0.50mol/L�̐��n�t��100mL���肽���B10�����_���n�t�͉�g�K�v���B (1)�@1.9���@(2)�@12mol/L�@(3)�@49g 3���̊e�₢�ɕ�������p���ē�����B (1)�@���ʃp�[�Z���g�Z�x��P�k���l�̗��_���n�t�̖��x��d�kg/cm3�l�ł������B���̗��_���n�t�̃����Z�x�͉�mol/L���B�������C���_�̕��q�ʂ�M�Ƃ���B (2)�@���q��M�̕����𐅂ɗn�������C�����Z�xc�kmol/L�l�ɂ������n�t������B���n�t�̖��x��d�kg/cm3�l�Ƃ��āC���̐��n�t�̎��ʃp�[�Z���g�Z�x�����߂�B (1)�@10dP/M�@(2)�@cM/10d |
|
 |
|